TUJUAN PERCOBAAN
- Mengetahui perubahan yang terjadi pada larutan glukosa, fruktosa, laktosa, pati dan maltosa pada uji molisch
- Mengetahui perubahan yang terjadi pada larutan pepton, gelatin, kasein, albumin dan fenol pada uji xantoprotein
- Mengetahui senyawa karbohidrat yang mengandung karbohidrat pada uji barfoed pada percobaan yang dilakukan
Karbohidrat adalah senyawa karbonil alami dengan beberapa gugus hidroksil. Senyawasenyawa ini menyusun sebagian besar bahan organik didunia karena peran multipelnya pada semua bentuk kehidupan. Pertama, karbohidrat bertindak sebagai sumber energi, bahan bakar, dan zat antara metabolisme Contohnya pati pada tumbuh-tumbuhan dan glikogen pada hewan. adalah polisakarida yang dapat dimobilisasi untuk menghasilkan glukosa, bahan bakar utama untuk pembentukan energi. ATP, sebagai alat tukar energi bebas yang universal adalah merupakan derivat gula terfosforilasi. Kedua gula ribosa dan deoksiribosa pembentuk sebagian kerangka struktur RNA dan DNA. Fleksibilitas cincin kedua gula ini penting pada penyimpanan dan ekspresi informasi genetik. Ketiga, polisakarida adalah elemen struktur dinding sel bakteri dan tumbuh-tumbuhan. Contohnya adalah selulosa suatu komponen utama dinding sel tumbuhtumbuhan yang merupakan satu senyawa organik yang melimpah ruah pada biosfer. Keempat,karbohidrat berikatan dengan banyak senyawa protein dan lipida. Misalnya, unit-unit gula glikofirin, suatu protein tunggal integral membran, memberi sel-sel darah merah satu lapisan anion yang sangat polar. Beberapa penelitian mengungkapkan bahwa unit-unit karbohidrat pada permukaan sel memainkan peranan kunci pada proses pengenalan antarsel.Karbohidrat yang berasal dari makanan, dalam tubuh mengalami perubahan atau metabolisme. Hasil metabolisme karbohidrat antara lain adalah glukosa yang terdapat dalam darah, sedangkan glikogen adalah karbohidrat yang disintesis dalam hati dan digunakan oleh selsel pada jaringan otot sebagai sumber energi. Contoh karbohidrat yang terdapat pada bahan makanan adalah amilum atau pati dan sukrosa (gula tebu).Energi yang terkandung dalam karbohidrat pada dasarnya berasal dari energi matahari. Karbohidrat dalam hal ini glukosa dibentuk dari karbon dioksida dan air dengan bantuan cahaya matahari dan klorofil dalam daun. Selanjutnya glukosa yang terjadi diubah menjadi amilum dan disimpan pada bagian lain seperti pada buah atau umbi. Karbohidrat atau sakarida terdapat gugus hidroksil (-OH), gugus aldehida atau gugus keton. Berdasarkan gugus-gugus fungsi yang ada tersebut maka karbohidrat dapat didefinisikan sebagai senyawa polihidroksialdehida atau polihidroksiketon, atau senyawa yang dihidrolisis dari keduanya. Sir Walter Norman Haworth (1883-1950), seorang ahli kimia berkebangsaan Inggris pada tahun 1937 memperoleh hadiah Nobel berpendapat bahwa pada molekul glukosa kelima atom karbon yang pertama dengan atom oksigen dapat membentuk cincin segi enam. Oleh karena itu diusulkan penulisan rumus struktur karbohidrat sebagai bentuk cincin furan atau piran. Atom karbon suatu molekul gula dinomori mulai dari ujung yang paling dekat dengan aldehida atau keton. Di dalam larutan pH netral, kurang dari 0,1% molekul gula mengandung gugus aldehida bebas. Penyebabnya adalah suatu reaksi antara gugus OH gula dengan gugus aldehida dari molekul gula yang sama. Gugus karbonil yang ada pada semua karbohidrat sangat reaktif dan dapat membentuk hemiasetal atau asetal dengan senyawa lain. Misalnya aldehida dapat bereaksi dengan alkohol ( X-OH) untuk membentuk hemiasetal. Sebagai suatu molekul polimer, karbohidrat digolongkan berdasarkan jumlah monomer penyusunnya. Ada tiga jenis karbohidrat berdasarkan penggolongan ini yaitu: Monosakarida, disakarida (oligosakarida), dan polisakarida.
Monosakarida, adalah senyawa karbohidrat yang paling sederhana yang tidak dapat dihidrolisis lagi. Umumnya senyawa ini adalah aldehida atau keton yang mempunyai dua atau lebih gugus hidroksil. Rumus kimia empiris karbohidrat adalah (CH2O)n dimana n = 3 atau lebih. Jika gugus karbonil pada ujung rantai monosakarida adalah turunan aldehida, maka monosakarida ini disebut aldosa. Dan bila gugusnya merupakan turunan keton maka monosakarida tersebut dinamakan ketosa. mosakarida yang paling kecil n = 3 adalah gliseraldehida dan dihidroksiaseton. Karbohidrat yang terbentuk dari dua sampai sepuluh monosakarida digolongkan dalam kelompok oligosakarida. Termasuk kelompok ini adalah disakarida, trisakarida dan seterusnya sesuai dengan jumlah satuan monosakaridanya. Disakarida terdiri dari dua monosakarida yang terikat, bila gugus hidroksi anomer dari suatu monosakarida diikatkan dengan ikatan glikosidik dengan gugus hidroksi gula lainnya.Tiga senyawa disakarida utama yang penting dan melimpah ruah dialam adalah sukrosa, laktosa dan maltosa. Ketiga senyawa ini memiliki rumus molekul yang sama (C12H22O11) tetapi struktur molekul berbeda. Dalam bahan makanan yang berasal dari tumbuh-tumbuhan, jeniskarbohidrat yang banyak digunakan adalah sukrosa yang bertindak sebagai cadangan karbohidrat yang larut.
Sukrosa atau gula tebu yang umum, didapatkan dari tebu atau bit. Atom-atom anomer unit glukosa dan unit fruktosa berikatan pada disakarida ini. Konfigurasi ikatan glikosidiknya adalah - untuk glukosa dan - untuk fruktosa. Dengan sendirinya sukrosa tidak mempunyai gugus pereduksi bebas (ujung aldehid atau keton), berbeda dengan sebagian besar gula lainnya. Hidrolisis sukrosa menjadi glukosa dan fruktosa dikatalisis oleh enzim sukrase (juga disebut invertase karena hidrolisis mengubah aktivitas optik dari putaran ke kanan menjadi ke kiri. Laktosa merupakan karbohidrat yang paling penting di dalam air susu mamalia. Di dalam susu sapi terdapat kurang lebih 4,5% laktosa dan air susu ibu mengandung hingga 7,5%. Laktosa terbentuk dari ikatan glikosida antara karbon nomor 1 pada galaktosa dan atom karbon nomor 4 pada glukosa ( ikatan glikosidik -1,4). Laktosa dihidrolisis menjadi glukosa dan galaktosa oleh enzim laktase pada manusia ( oleh -galaktosidase pada bakteri). Maltosa terbentuk antara dua unit glukosa berikatan melalui ikatan glikosidik -1,4. Maltosa atau biasa disebut gula gandum berasal dari hidrolisis pati dan kembali dihidrolisis menjadi glukosa oleh maltase. Selobiosa juga tersusun dari dua monosakarida glukosa yang berikatan glikosida antara karbon nomor 1 dan 4. Polisakarida merupakan karbohidrat bentuk polimer dari satuan monosakarida yang sangat panjang. Polisakarida terdapat dimana-mana di dalam alam. Polisakarida berfungsi sebagai : struktural (bahan bangunan), bahan makanan (polisakarida cadangan), dan sebagaizat spesifik. Contoh polisakarida adalah selulosa, pati (amilum), asam hialuronik, glikogen dan lain sebagainya.
Asam amino adalah unit monomerik yang membentuk protein, dan asam amino adalah produk primer penguraian protein. Bila protein dipanaskan dalam suasana asam atau basa kuat, maka ikatan kovalen yang menghubungkan asam amino satu dengan yang lainnya akan terputus, alhasil kita akan mendapatkan molekul-molekul yang relatif lebih sederhana yaitu asam amino. Asam amino yang petama kali diisolasi adalah aspargin yang ditemukan pada tahun 1806. sedangkan asam amino yang paling akhir diisolasi adalah treonin, baru ditemukan pada tahun 1938. semua asam amino mempunyai nama umum (trivial). Protein adalah suatu polipeptida yang mempunyai bobot molekul yang sangat bervariasi, dari 5000 hingga lebih dari satu juta. Mempunyai sifat yang berbeda-beda, ada protein yang mudah larut dalam air seperti bagian dalam putih telur (albumin), ada juga yang sukar larut dalam air contohnya rambut dan kuku adalah suatu protein yang tidak larut dalam air dan tidak mudah bereaksi. Peptida tersusun dari beberapa asam amino dan merupakan rantai dimana gugus karboksil asam amino yang satu dihubungkan dengan gugus amino dari asam amino lainnya melalui suatu ikatan peptida. Sintesis ikatan peptida ini terjadi dalam sel melalui suatu tahapan reaksi yang sangat kompleks. Ikatan peptida dibentuk melalui penghilangan molekul air dari penggabungan gugus karboksilat dari suatu asam amino dengan gugus amino dari asam amino lain.Dua asam amino yang dihubungkan oleh ikatan peptida disebut dipeptida, peptida yang terdiri dari 3 asam amino disebut tripeptida dan seterusnya. Apabila peptida mengandung lebih 10 asam amino disebut polipeptida. Suatu oligopeptida terdiri 4 asam amino dapat dilihat pada gambar dimana adanya ujung terminal karboksil ( -COOH ) dan ujung terminal amino (-NH2). Jika peptida disusun oleh asam-asam amino netral maka yang berionisasi hanya gugus karboksil dan gugus amino yang ada dikedua ujung saja. Tetapi jika peptida disusun oleh asam-asam amino yang bersifat basa atau asam, ionisasinya juga terdapat pada bagian lain dari molekul. Dan gugus ini dapat aktif dan berfungsi.
Meskipun struktur primer protein merupakan rantai linier, hampir semua protein dialam dijumpai dalam bentuk melipat menjadi bentuk yang lebih kompak dapat berupa elip atau bulat membentuk molekul globular. Di alam terdapat dua macam protein yakni protein globular dan protein serabut ( fibrosa).Protein fibrosa erat hubungannya dengan unsur-unsur yang membangun sel dan berkaitan dengan sifat-sifat khas sel. Artinya protein ini terdiri dari peptida berantai panjang dan berupa serat-serat yang tersusun memanjang, dihubungkan secara lateral oleh beberapa ikatan silang. Sifatnya kurang larut, bersifa amorf, dapat memanjang dan berkontraksi. Contohnya ialah keratin, miosin, kolagen. Protein serabut dapat dibagi atas heliks, triple heliks dan - pleated sheet yang paralel dan antiparalel (Ischak dkk.,2017).
ALAT
BAHAN

PROSEDUR KERJA
Uji molish
Sampel kentang
- Dimasukkan ke dalam 6 buah tabung reaksi berturut-turut 5 ml larutan glukosa larutan fruktosa larutan sukrosa larutan laktosa larutan Pati dan larutan maltosa
- Ditambahkan 4 tetes pereaksi molisch ke dalam masing-masing tabung dan aduk dengan baik
- Ditambahkan perlahan-lahan melalui dinding tabung 3 ml asam sulfat pekat dan diperhatikan perubahan warna yang terjadi
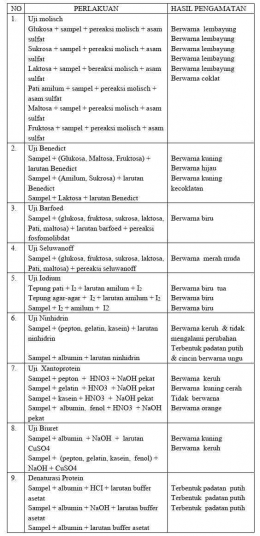
Hasil pengamatan
- Glukosa, sukrosa, maltosa, laktosa, pati : menghasilkan perubahan warna keunguan menjadi lembayung dengan sampel bereaksi
- Fruktosa : menghasilkan perubahan warna menjadi coklat
Uji Benedict
Sampel kentang
- Dimasukkan ke dalam 6 buah tabung reaksi dan dimasukkan masing-masing 5 ml larutan Benedict
- Ditambahkan 8 tetes larutan glukosa fruktosa sukrosa laktosa Pati dan maltosa berturut-turut ke dalam tabung 1 sampai tabung 7
- Dipanaskan campuran tersebut dalam penangas air selama 5 menit dan dibiarkan sampai dingin
- Dicatat perubahan yang terjadi
Hasil pengamatan
- Glukosa, maltosa, fruktosa : menghasilkan perubahan warna menjadi kuning
- Amilum dan sukrosa : menghasilkan perubahan warna menjadi hijau
- Laktosa : menghasilkan perubahan warna menjadi kuning kecoklatan dengan terlaruT
- Uji Barfoed
Sampel kentang
- Di dalam 6 buah tabung reaksi dimasukkan masing-masing 1 ml larutan barfoed
- Ditambahkan berturut-turut 1 mili larutan glukosa larutan fruktosa sukrosa laktosa Pati dan maltosa
- Dipanaskan campuran tersebut dalam penangas air selama 5 menit dan biarkan menjadi dingin perhatikan perubahan yang terjadi
- Ditambahkan 1 ml pereaksi fosfomaliodat ke dalam campuran tersebut dikocok dan amati perubahan yang terjadi
Hasil pengamatan
- Glukosa, fruktosa, maltosa, sukrosa, laktosa, pati + sampel + barfoed dan dipanaskan sampai dingin : menghasilkan warna biru muda yang terlihat pudar
- Fosfomolibdat : menghasilkan warna biru jelas
Uji seliwanoff
Sampel kentang
- Dimasukkan masing-masing Pemilu pereaksi seliwanof ke dalam 6 buah tabung reaksi
- Ditambahkan 8 tetes larutan glukosa fruktosa sukrosa maltosa Pati dan laktosa ke dalam tabung 1 sampai 6 secara berturut-turut
- Dipanaskan campuran tersebut dalam penanganan air selama 1 menit dan diperhatikan perubahan yang terjadi
Hasil Pengamatan
*Glukosa, fruktosa, sukrosa, maltosa, pati dan laktosa + sampel + seliwanoff : menghasilkan warna yang keruh dan warna yang tidak jelas
*Dipanaskan dan didinginkan : menghasilkan warna merah muda yang jelas terlihat
Uji iodium
Sampel kentang
- Dimasukkan secara berturut-turut sedikit tepung pati dan tepung agar-agar ke dalam dua tabung reaksi
- Ditambahkan 4 tetes larutan iodium
- Dicampurkan hingga merata diperhatikan warna yang terjadi
- Dimasukkan 2 ml larutan amilum 2% ke dalam tabung reaksi Kemudian ditambahkan 5 tetes larutan iodium dan diperhatikan warna yang terjadi
- Dipanaskan tabung reaksi beberapa menit dan diamati perubahan yang terjadi kemudian didinginkan
Hasil pengamatan
*Pati + I2 + sampel : berwarna biru + amilum + I2 : berwarna biru tua, dipanaskan tidak berwarna
*Tepung agar-agar + sampel + I2 : berwarna hijau + amilum + I2 : berwarna biru, dipanaskan tidak berwarna
*Sampel + I2 : berwarna biru + amilum + I2 : berwarna biru, dipanaskan tidak berwarna
uji ninhidrin
Sampel tahu
- Dimasukkan berturut-turut 3 ml larutan albumin gelatin kasein dan pepton ke dalam empat tabung reaksi
- Ditambahkan 0,5 ml larutan ninhidrin 1% untuk setiap tabung
- Dipanaskan ke dalam penangas air mendidih selama 10 menit dan diperhatikan perubahan warna yang terjadi
Hasil pengamatan
*Albumin : sebelum pemanasan berwarna keruh, setelah pemanasan terbentuk padatan yang berwarna putih dan diatasnya ada cincin yang berwarna ungu
*Pepton, gelatin, kasein : sebelum dan sesudah pemanasan tidak terjadi perubahan dan warnanya tetap keruh
uji xantoprotein
Sampel tahu
- Dimasukkan berturut-turut 2 ml larutan albumin gelatin kasein pepton dan fenol ke dalam 5 tabung reaksi
- ditambahkan 1 ml HNO3 pekat ke setiap tabung dicampurkan dan dipanaskan dengan hati-hati dan diperhatikan warna yang terjadi
- ditambahkan setetes dimensi tetes Larutan natrium hidroksida pekat hingga larutan menjadi basa setelah dingin dan amati perubahan yang terjadi
HASIL PENGAMATAN
*Pepton + 1ml HNO3 pekat lalu dipanaskan menjadi keruh dan ditambahkan 4 tetes NaOH tetap keruh
*Gelatin + 1ml HNO3 pekat lalu dipanaskan menjadi kuning cerah dan ditambahkan 4 tetes NaOH tetap berwarna kuning cerah
*Kasein + 1ml HNO3 pekat lalu dipanaskan menjadi bening dan ditambah 4 tetes NaOH tetap bening (tidak berwarna)
*Albumin + 1ml HNO3 pekat lalu dipanaskan menjadi warna kuning dan ada endapan berwarna putih, setelah ditambah 4 tetes NaOH menjadi warna orange
*Fenol + 1ml HNO3 pekat lalu dipanaskan menjadi warna kuning tua dan setelah ditambah 4 tetes NaOH menjadi warna orange
Uji buret
Sampel tahu
- Dimasukkan berturut-turut 3 mili larutan albumin gelatin kasein pepton dan fenol ke dalam 5 buah tabung reaksi
- ditambahkan 1 ml natrium hidroksida 10% ke setiap tabung lalu dikocok
- ditambahkan 2 tetes larutan CuSO4 0,1% dan dikocok
- ditambahkan setengah tetes CuSO4 0,1%. Jika timbul warna dan diamati perubahan yang terjadi
Hasil pengamatan
* Albumin + 1ml NaOH menjadi keruh dan setelah ditambah 4 tetes CuSO4 menjadi warna kuning
* Pepton,gelatin, kasein, fenol + 1ml NaOH menjadi keruh + 4 tetes CuSO4 tetep warna keruh
Denaturasi Protein
Sampel tahu
- Disediakan tiga tabung reaksi dibuat campuran larutanDengan larutan albumin ke dalam tabung 1 2 3 dimana Larutan buffer asetat ke dalam tabung 3 sebanyak 1 mlLarutan HCL ke dalam tabung 1 sebanyak 1 ml Larutan natrium hidroksida ke dalam tabung 2 sebanyak satu ml
- Di tempat kan ketika tamu reaksi tersebut ke dalam air mendidih selama 15 menit
- didinginkan dan diperhatikan apa yang terjadi ditambahkan 10 ml larutan buffer asetat PH 4,7 ke dalam tabung 1 dan 2 dan diamati perubahan yang terjadi
Hasil pengamatan
*Tabung 1 : dipanaskan terbentuk endapan putih
*Tabung 2 : dipanaskan terbentuk endapan putih
*Tabung 3 : dipanaskan terbentuk endapan putih
Setelah dingin + 10ml buffer asetat
*Tabung 1 : tidak terjadi perubahan, tetap terbentuk endapan putih
*Tabung 2 : tidak terjadi perubahan, tetap terbentuk endapan putih
HASIL PENGAMATAN

PEMBAHASAN
Pereaksi molisch terdiri dari -naftol dalam alkohol yang akan bereaksi dengan furfural membentuk senyawa kompleks berwarna ungu yang disebabkan oleh daya dehidrasi asam sulfat pekat terhadap karbohidrat dan akan membentuk cincin berwarna ungu pada larutan glukosa, sukrosa, laktosa, maltosa, arabinosa, dan selulosa. Tujuan ditambahkannya asam sulfat pekat adalah untuk menghidrolisis ikatan pada sakarida agar menghasilkan furfural. Pada prinsip uji iodin berguna untuk menentukan adanya gugus polisakarida dan untuk mengetahui pembentukan kompleks pati-iodium. Jika suatu senyawa mengandung polisakarida dan ditambah dengan iodium, maka akan membentuk kompleks adsorpsi berwarna yang spesifik. Uji Benedict bertujuan untuk mengidentifikasi gula pereduksi, dimana gugus perduksinya merupakan aldehid dan keton. Prinsipnya adalah larutan CuSO4 dalam suasana alkali direaksikan dengan gula pereduksi sehingga Cu2+ tereduksi menjadi Cu+ berwarna merah bata. Fungsi dari CuSO4 adalah sebagai oksidator yang bersifat basa lemah dan fungsi Na-sitrat adalah sebagai zat pencegah pembentukan Cu(OH)2. Uji barfoed memiliki prinsip yang sama seperti dengan uji yaitu reduksi Cu2+ menjadi Cu+ oleh karbohidrat yang mengandung aldehid dan keton bebas. Uji seliwanoff bertujuan membuktikan adanya ketosa (fruktosa), dengan prinsip konversi fruktosa menjadi asam levulinat dan hidroksimetilfurfural yang kemudian dikondensasikan dengan resorsinol. 214PAGE 1Hasil Uji BiuretPereaksi uji Biuret digunakan untuk mendeteksi adanya ikatan peptida pada zat uji. Adanya ikatan peptida menandakan adanya protein karena asam amino berikatan dengan asam amino lain melalui ikatan peptida yang akan membentuk protein [2]. Sebanyak 2 mL larutan uji ditambahkan dengan 1 mL NaOH 10%. Fungsi dari NaOH yaitu mencegah endapan Cu(OH)2, dan memecah ikatan protein menjadi urea, sebagai katalisator. Selanjutnya penambahan 2-3 tetes larutan CuSO4 yang berfungsi sebagai pendonor Cu2+. Jika terbentuk warna ungu atau merah menunjukkan hasil positif dan jika terbentuk warna biru berarti negatif. Pada uji ninhidrin digunakan untuk identifikasi asam amino bebas yang terdapat dalam sampel. Reagen ninhidrin merupakan hidrat triketon siklik dan bila bereaksi dengan asam amino menghasilkan zat warna ungu. Hanya atom nitrogen pewarna ungu yang berasal dari asam amino, sisanya menjadi aldehida dan karbon dioksida [20]. Pemanasan yang dilakukan pada tiap uji percobaan bertujuan untuk koagulasi protein sehingga tidak dapat larut dalam air dan terbentuknya endapan . Uji xantoprotein bertujuan untuk menunjukan adanya inti benzene (cincin fenil) atau senyawa aromatik pada suatu sampel protein dan untuk mendeteksi asam amino yang mengandung inti aromatik, seperti tirosin, triptofan, dan fenilalanin, dalam larutan protein. Indikator pengamatan dari uji ini akan mengubah sampel menjadi endapan berwarna kuning atau larutan kuning. Cincin benzene aromatik dalam asam amino ini mengalami nitratasi ketika dipanaskan dengan asam nitrat pekat (HNO3), sehingga terbentuk turunan nitro berwarna kuning (Panjaitan dkk.,2023).
Berdasarkan pengamatan yang dilakukan diperoleh bahwa
- pada uji molisch sampel kentang yang dicampurkan dengan glukosa sukrosa maltosa laktosa dan Pati menghasilkan warna Lembayung sehingga sampel kentang termasuk positif mengandung karbohidrat
- Pada uji Benedict dengan mencampurkan sampel kentang dengan glukosa maltosa dan fruktosa menghasilkan warna kuning sedangkan amilum dan sukrosa menghasilkan warna hijau dan laktosa menghasilkan warna kuning kecoklatan yang terlarut sehingga pada uji Benedict kentang tidak termasuk mengandung karbohidrat
- Pada uji barcode dengan mencampurkan sampel kentang dengan glukosa fruktosa sukrosa lactosapati maltosa dan barcode menghasilkan warna biru dan di validasi dengan menambahkan pereaksi fosfomalibat menghasilkan warna biru yang pekat menunjukkan bahwa menurut percobaan uji barcode sampel kentang positif mengandung karbohidrat
- Pada uji seliwanoff dengan mencampurkan sampel kentang dengan glukosa fruktosa sukrosa maltosa Pati dan laktosa dengan pereaksi seliwanoff menghasilkan warna keruh dan didinginkan setelah dipanaskan menghasilkan warna merah muda menunjukkan kentang mengandung karbohidrat
- Pada uji iodium dengan menambahkan Pati tepung agar-agar dan sampel kentang menunjukkan bahwa pada Pati menunjukkan adanya warna biru pada tepung agar-agar menunjukkan adanya warna biru dan pada kentang menunjukkan adanya warna biru membuktikan bahwa menurut uji iodium sampel kentang mengandung karbohidrat
- Pada uji ninhidrin ketika sampel tahu dicampur kan dengan albumin yang menghasilkan warna ungu dan dicampurkan dengan pepton gelatin dan kasein tidak mengalami perubahan dan terdapat keruh menunjukkan bahwa albumin yaitu putih telur dengan sampel tahu termasuk positif mengandung protein
- Pada uji xanto protein di mana sampel tahu yang dicampur kan dengan gelatin menghasilkan warna kuning cerah dicampurkan dengan pepton menghasilkan warna keruh kasein menimbulkan tidak berwarna dan albumin menghasilkan warna orange dan begitu juga dengan fenol membuktikan bahwa menurut uji satu protein sampel tahu mengandung inti benzen yang di mana mengandung positif protein
- Pada uji biuret ketika sampel tahu dicampurkan dengan albumin menghasilkan warna kuning dan dicampur kan dengan pepton gelatin kasein dan fenol menghasilkan warna keruh menunjukkan bahwa pada uji biuret tidak terdapat hasil yang signifikan
- Ada uji denaturasi protein dengan mencampurkan albumin dengan HCL menimbulkan padatan putih mencampurkan albumin dengan NaOH menimbulkan padatan putih dan albumin dengan buffer asetat menimbulkan endapan putih menunjukkan bahwa protein dengan adanya asam amino terdenaturasi
KESIMPULAN
- Pada uji molisch yang menghidrolisis ikatan sakarida menghasilkan pulvular diperoleh pada pereaksi larutan glukosa, sukrosa, maltosa, laktosa dan pati menghasilkan warna lembayung yang menunjukkan terkandungnya karbohidrat pada larutan tersebut. Sedangkan berdasarkan percobaan yang dilakukan fruktosa tidak mengandung hal yang sama dikarenakan berubah warna menjadi coklat.
- Pada uji xantroprotein yang menunjukkan adanya inti benzena mendeteksi asam amino diperoleh pada sampel protein yang direaksikan dengan pepton dan kasein menghasilkan tidak berwarna, sampel protein yang direaksikan dengan gelatin menghasilkan warna kuning menunjukkan terkandungnya protein dan sampel protein yang direaksikan dengan albumin dan fenol menghasilkan warna orange yang menunjukkan terkandungnya asam amino dan terbentuknya inti benzene.
- Pada uji barfoed jenis larutan yang menunjukkan terkandung karbohidrat adalah pada larutan glukosa, fruktosa, sukrosa, laktosa, pati dan maltosa yang direaksikan dengan sampel akan menunjukkan kandungannya karbohidrat memiliki reaktivitas yang tinggi dan sampel mengandung gugus aldehid.

Follow Instagram @kompasianacom juga Tiktok @kompasiana biar nggak ketinggalan event seru komunitas dan tips dapat cuan dari Kompasiana
Baca juga cerita inspiratif langsung dari smartphone kamu dengan bergabung di WhatsApp Channel Kompasiana di SINI