* Distilasi adalah suatu cara pemisahan larutan dengan menggunakan panas sebagai pemisah atau "separating agent". Jika larutan yang terdiri dari dua buah komponen yang cukup mudah menguap, misalnya larutan benzena-toluena, larutan n-Heptan dan n-Heksan dan larutan lain yang sejenis didihkan, maka fase uap yang terbentuk akan mengandung komponen yang lebih menguap dalam jumlah yang relatif lebih banyak dibandingkan dengan fase cair.
Jadi ada perbedaan komposisi antara fase cair dan fase uap, dan hal ini merupakan syarat utama supaya pemisahan dengan distilasi dapat dilakukan. Kalau komposisi fase uap sama dengan komposisi fase cair, maka pemisahan dengan jalan distilasi tidak dapat dilakukan.
Dasar pemisahan pada destilasi adalah perbedaan titik didih komponen cairan yang dipisahkan pada tekanan tertentu. Penguapan diferensial dari suatu campuran cairan merupakan bagian terpenting dalam proses pemisahan dengan destilasi, diikuti dengan penampungan material uap dengan cara pendinginan dan pengembunan dalam kondensor pendingin-air.
Mempelajari proses pemisahan dengan teknik destilasi mesti dipahami bahwa semua molekul dalam fasa cair memilika dinamika pergerakan yang konstan. Pembangkitan tekanan internal dan kecenderungan molekul lepas dari permukaan dalam bentuk uap, tergantung pada karakteristik cairan. Tekanan uap adalah ukuran kecenderungan terlepasnya molekul dari permukaan cairan, tekanan uap cairan adalah sifat dari cairan itu dan tidak tergantung pada komposisi fasa uap. Peningkatan temperatur akan meningkatkan pergerakan molekul fasa cair sehingga mempercepat proses terlepasnya molekul.
* Volatilitas adalah kecenderungan suatu zat untuk menguap. Zat yang mudah menguap memiliki kemampuan untuk masuk ke fase uap. Hal ini dapat terjadi selama pemanasan atau tanpa pemanasan. Volatilitas dan tekanan uap suatu zat saling berhubungan. Jika volatilitasnya tinggi maka tekanan uapnya juga tinggi. Sebaliknya, jika volatilitasnya rendah, maka tekanan uapnya pun rendah. Biasanya cairan bersifat mudah menguap. Mereka cenderung masuk ke fase uap dengan cepat. Misalnya aseton, heksana, kloroform adalah cairan yang mudah menguap dan cepat menguap. Apalagi ada beberapa padatan yang bisa langsung masuk ke fasa uap tanpa melalui fasa cair.
Zat non volatil adalah zat yang tidak dapat menguap dengan cepat. Mereka tidak memiliki tekanan uap yang lebih tinggi pada suhu dan tekanan ruangan normal. Selain itu, zat yang tidak mudah menguap sebagian besar akan berbentuk padat pada suhu ruangan. Misalnya natrium klorida, perak nitrat merupakan senyawa yang tidak mudah menguap. Terlebih lagi, ketika senyawa nonvolatil bercampur dengan cairan yang mudah menguap seperti air, senyawa tersebut mudah dipisahkan melalui penguapan. Kemudian cairan yang mudah menguap akan menguap meninggalkan padatan yang tidak mudah menguap di dasar wadah.
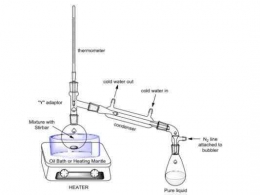
BERIKUT RANGKAIAN ALAT DESTILASI
PENENTUAN KOEFISIEN DISTRIBUSI DAN PERSEN EKSTRAKSI
* Menurut Soebagio (2002:34), menurut hukum distribusi Nerst, bila ke dalam kedua pelarut yang tidak saling bercampur dimasukkan solut yang dapat larut dalam kedua pelarut tersebut maka akan terjadi pembagian kelarutan. Kedua pelarut tersebut umumnya pelarut organik dan air. Dalam praktek solut akan terdistribusi dengan sendirinya ke dalam dua pelarut tersebut setelah di kocok dan dibiarkan terpisah. Perbandingan konsentrasi solut di dalam kedua pelarut tersebut tetap, dan merupakan suatu tetapan pada suhu tetap. Tetapan tersebut disebut tetapan distribusi atau koefisien distribusi. Koefisien distribusi dinyatakan dengan berbagai rumus sebagai berikut :
KD = atau KD =
dari rumus tersebut jika harga KD besar, solute secara kuantitatif akan cenderung terdistribusi lebih banyak ke dalam pelarut organik begitu pula sebaliknya. Rumus tersebut hanya berlaku bila:
a. Solute tidak terionisasi dalam salah satu pelarut
b. Solute tidak berasosiasi dalam salah satu pelarut
c. Zat terlarut tidak dapar bereaksi dengan salah satu pelarut atau adanya reaksi- reaksi lain.
* Menurut Pudjaatmaka (2002:312-213). Hukum distribusi merupakan hukum pembagian jumlah molekul menurut tingkatan energinya atau secara umum distribusi adalah jumlah cara untuk merealisasikan pembagian (distribution law). Tujuan ekstraksi yaitu untuk menarik atau memisahkan senyawa dari simplisia atau campurannya. Pemilihan metode dilakukan dengan memperhatikan senyawa, pelarut yang digunakan serta alat yang tersedia. Metode ekstraksi yang umum digunakan adalah maserasi dan refluks (Hanani, 2017).
* Zat cair dan zat padat berbeda dengan gas, dimana perbedaannya adalah, pada molekul-molekul zat cair atau zat padat terjadi ikatan yang sangat kuat antar molekulnya. Untuk memperoleh larutan, suatu solven harus mengalahkan ikatan yang kuat pada solut sehingga molekul-molekul solven mendapatkan tempat. Sebaliknya pada saat yang bersamaan molekul-molekul solven itu sendiri harus dapat dipisahkan satu dengan lainnya oleh molekul-molekul solut. Fenomena ini terjadi kalau gaya tarik menarik antara molekul kedua komponen tersebut adalah sama.
* Proses ekstraksi dapat menggunakan 3 jenis pelarut dengan tingkat kepolaran yang berbeda, yaitu n- heksana (nonpolar), etil asetat (semipolar) dan etanol/metanol (polar). Perbedaan pelarut dalam ekstraksi dapat mempengaruhi kandungan total senyawa bioaktif (Santoso et al., 2012). Pemilihan metode ekstraksi tergantung pada sifat bahan dan senyawa yang akan diisolasi. Ada beberapa teknik ekstraksi padat-cair yang tersedia. Teknik konvensional yang umum digunakan adalah ekstraksi perendaman (maserasi) ekstraksi soxhlet dan perkolasi.
PEMISAHAN WARNA TINTA DAN ION ION LOGAM SECARA KROMATOGRAFI KERTAS
* Kromatografi adalah proses melewatkan sampel melalui suatu kolom. Perbedaan kemampuan adsorbsi terhadap zat-zat yang sangat mirip mempengaruhi resolusi zat terlarut dan menghasilkan apa yang disebut kromatogram (Khopkar, 2003 : 130).
Kromatografi kertas merupakan bidang khusus kromatografi cair-cair. Fase diam berupa lapisan tipis air yang terserap oleh kertas. Selain airdapat juga dipakai cairan lain. Pengerjaannya sangatsederhana. Penempatan satu tetes larutan cupl;ikan pada ujung kertasdan kemudian mencelupkannya ke dalam pelarut (eluen) sudah cukup untuk memisahkan komponen-komponen cuplikan (Soebagio, 2003 : 59).
* Mekanisme pemisahan dengan kromatografi kertas prinsipnya sama dengan mekanisme pada kromatografi kolom. Adsorben dalam kromatografi kertas adalah kertas saring yakni selulosa. Sampel yang akan dianalisis ditotolkan ke ujung kertas yang kemudian digantung dalam wadah. Kemudian dasar kertas saring dicelupkan ke dalam pelarut yang mengisi dasar wadah. Fasa mobil (pelarut) dapat saja beragam. Air, etanol, asam asetat atau campuran zat-zat ini dapat digunakan (Wawan, 2009).
* Fase diam merupakan lapisan cairan pelarut (pengembang) yang teradsorpsi pada permukaan kertas, sedangkan fase gerak merupakan bagian pelarut (pengembang,eluen) yang berfungsi menggerakkan komponen (Arief Pambudi, et.al., 2014).
IDENTIFIKASI ZAT WARNA DALAM MAKANAN/ MINUMAN DENGAN KROMATOGRAFI KERTAS
* Berdasarkan arahnya, kromatografi kertas terbagi atas dua yaitu kromatografi kertas satu arah dan kromatografi kertas dua arah. Kromatografi kertas satu arah ialah kromatografi yang fase diam didalamnya adalah kertas serap yang sangat seragam, fase geraknya pelarut yang sesuai. Pewarna diteteskan pada garis yang sama kemudian ditaruh didalam pelarut yang sesuai. Dengan jumlah yang minimum. Kerta digantungkan pada wadah berisi lapisan tipis pelarut. Batas atas dikaitkan pada atas wadah hingga terelusikan naik. Sedangkan juga terdapat kromatografi kertas satu arah yang lain yang arahnya menurun, disebut dengan metode descending (Sastrohamidjojo, 1985).
* Analisis sampel zat warna dengan kromatografi kertas pada sampel zat warna dan sampel zat warna sintetik digunakan warna pembanding. Berdasarkan arahnya kromatografi kertas dapat dilakukan dengan tiga metode, yaitu; metode ascending (menaik), descending (menurun) dan metode radial (mendatar). Kromatografi ascending merupakan kromatografi kertas yang arah fase geraknya menaik, dengan memanfaatkan gaya kapiler. Sedangkan pada kromatografi descending dalam pelaksanaannya memanfaatkan gaya gravitasi sehingga arah fase geraknya menurun. Dan, pada kromatografi radial, memanfaatkan bentuk bulat dari kertas, komponen-komponen akan dielusikan melingkar (Khopkar, 1990).
* Dalam mengidentifikasi noda-noda sangat lazim menggunakan harga Rf (Retordation factor). Cara paling mudah dalam pengukuran Rf adalah dengan menggunakan mistar. Namun ada cara lain untuk mengidentifikasi senyawa-senyawa yaitu dengan reaksi-reaksi warna yang karakteristik. Reaksi kenayakan sangat berguna dalam pemisahan senyawa-senyawa anorganik, tetapi untuk senyawa organik sangat kecil kejadiannya, karena kebanyakan konstituen-konstituen dari campuran mempunyai sifat-sifat kimia yang mirip (Wertheim, 2000).
* Harga Rf mengukur kecepatan bergeraknya zona realatif terhadap garis depan pengembang. Nilai Rf di definisikan oleh hubungan:
Nilai Rf menunjukkan identitas suatu zat yang dicari sehingga nilai Rf harus sama, baik pada descending maupun ascending. Rf adalah sarana terpenting dalam memaparkan dan membedakan pigmen yang satu dengan pigmen yang lain (Khopkar, 1990).
PEMISAHAN KOMPONEN DARI KUNYIT SECARA KROMATOGRAFI KOLOM
* Kromatografi kolom merupakan teknik kromatografi yang paling awal yang pertamakali di lakukan oleh D.T.Davy yaitu untuk membedakan komposisi minyak bumi. Ditinjau dari mekanismenya kromatografi kolom merupakan kromatografi serapan atau adsorbsi. Pemisahan kromatografi kolom adsorpsi didasarkan pada adsorpsi komponen-komponen campuran dengan afinitas berbeda-beda terhadap permukaan fase diam. Kromatografi kolom adsorpsi termasuk pada cara pemisahan cair-padat. Substrat padat (adsorben) bertindak sebagai fase diam yang sifatnya tidak larut dalam fase cair. Fase bergeraknya adalah cairan (pelarut) yang mengalir membawa komponen campuran sepanjang kolom.
* Sebagian besar prinsip pemisahan kromatografi kolom didasarkan pada afinitas kepolaran analit dengan fase diam, sedangkan fase gerak selalu memiliki kepolaran yang berbeda dengan fase diam. Pada Sebagian besar kromatografi kolom menggunakan fase diam yang bersifat polar dengan fase gerak yang non polar dengan begitu waktu retensi akan menjadi lebih singkat. Semakin cepat pergerakan fase gerak akan meminimalkan waktu yang diperlukan untuk bergerak di sepanjang kolom.
* Dalam kromatografi kolom, campuran dilarutkan dalam pelarut dan dituangkan ke dalam kolom yang berisi bahan padat. Komponen berbeda dalam campuran mengalir keluar kolom dengan kecepatan berbeda tergantung pada adsorpsinya terhadap bahan padat. jika kita menaruh sampel terlalu banyak dalam suatu spot, maka akan terjadi overload (luber) dan batas antar komponen akan saling tumpang tindih (overlap) dengan hasil yang terpisahkan dari spot dan akan saling terkontaminasi dengan komponen lainnya.
PEMISAHAN ZAT HIJAU DAUN DENGAN KROMATOGRAFI LAPIS TIPIS
* KLT termasuk dalam kategori kromatografi planar, selain kromatografi kertas. Kromatografi juga merupakan analisis cepat yang memerlukan bahan sangat sedikit, baik penyerap maupun cuplikannya. KLT dapat digunakan untuk memisahkan senyawa-senyawa yang sifatnya hidrofobik seperti lipida-lipida dan hidrokarbon yang sukar dikerjakan dengan kromatografi kertas.
* KLT juga dapat berguna untuk mencari eluen untuk kromatografi kolom, analisis fraksi yang diperoleh dari kromatografi kolom, identifikasi senyawa secara kromatografi, dan isolasi senyawa murni skala kecil (Gholib Ibnu & Abdul Rohman 2007).
* Prinsip KLT adalah adsorbsi dan partisi dimana adsorbsi adalah penyerapan pada pemukaan, sedangkan partisi adalah penyebaran atau kemampuan suatu zat yang ada dalam larutan untuk berpisah kedalam pelarut yang digunakan. Kecepatan gerak senyawa-senyawa ke atas pada lempengan tergantung pada (Sudarmadji dkk 2007) :
A. Bagaimana kelarutan senyawa dalam pelarut, hal ini bergantung pada bagaimana besar atraksi antara molekul-molekul senyawa dengan pelarut.
B. Bagaimana senyawa melekat pada fase diam, misalnya gel silika. Hal ini tergantung pada bagaimana besar atraksi antara senyawa dengan gel silika.
* Derajat retensi pada kromatografi lempeng biasanya dinyatakan sebagai faktor resensi. Pada fase diam, jika dilihat mekanisme pemisahan, fase diam dikelompokkan (Gritter Roy dkk 1991) :
A. Kromatogarfi serapan (Silika gel, alumina).
B. Kromatografi partisi (Selulosa, keiselguhr, silika gel).
C. Kromatografi penukar ion (Penukar ion selulosa, resina).
D. Kromatografi gel (Sephadex, Biogel).
Baca konten-konten menarik Kompasiana langsung dari smartphone kamu. Follow channel WhatsApp Kompasiana sekarang di sini: https://whatsapp.com/channel/0029VaYjYaL4Spk7WflFYJ2H