Di rumah kita pastinya banyak terdapat perkakas dan peralatan rumah tangga, bukan? Mari kita perhatikan bahan dasar logam penyusun perkakas dan peralatan di sekitar rumah kita itu. Pastinya beragam. Ada yang terbuat dari besi, baja, aluminium atau stainless steel.
Untuk memahami penggunaan logam sebagai peralatan atau perkakas rumah tangga, maka kita harus memperhatikan karakteristik dari logam yang kita gunakan itu. Salah satu karakteristik logam yang perlu diperhatikan adalah kemampuan logam bertahan untuk tidak cepat berkarat.
Proses Korosi
Pengaratan logam adalah peristiwa kimiawi yang sering terjadi di dalam kehidupan. Dalam ilmu Kimia, peristiwa ini disebut dengan istilah korosi. Korosi terjadi disebabkan karena terjadinya reaksi reduksi oksidasi (redoks) pada logam yang berinteraksi dengan material lain yang ada di lingkungan.
Pada proses korosi, logam akan mengalami oksidasi, dan material yang lain menjadi pemicunya, atau biasa disebut material oksidator. Oksidator sendiri akan mengalami reaksi reduksi. Logam dan material oksidator yang mengoksidasinya, terdapat dalam sebuah sistem elektrokimia yang memungkinkan terjadinya aliran elektron.
Aliran elektron terjadi karena adanya perbedaan potensial reduksi pada kedua material. Prinsip kerjanya mengikuti prinsip kerja yang terjadi pada sel volta. Seperti kita ketahui, pada sel volta material yang memiliki potensial reduksi tinggi akan mengalami reduksi dan menjadi katoda (kutub positif). Sedangkan material yang memiliki potensial reduksi rendah akan mengalami oksidasi dan menjadi anoda (kutub negatif).
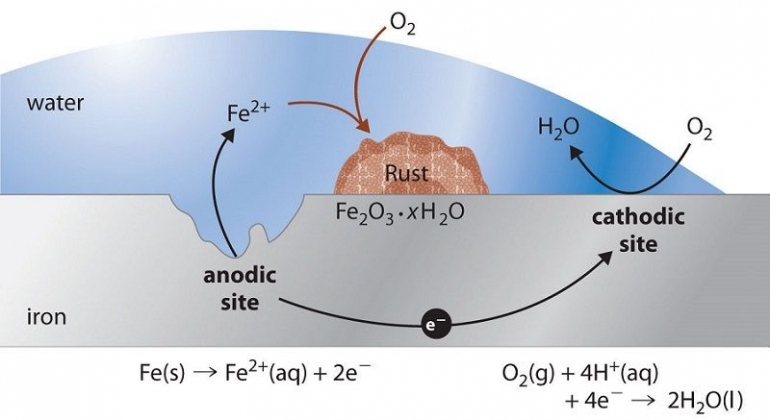
Ketika kita perhatikan isi rumah kita, besi adalah logam yang paling banyak digunakan. Namun, yang menjadi permasalahan adalah besi sangat rentan sekali mengalami korosi. Besi yang berada di lingkungan akan berinteraksi dengan oksigen di udara dan juga molekul air. Interaksi ini yang kemudian menjadi penyebab terjadinya korosi.
Pada peristiwa korosi besi, besi akan teroksidasi membentuk ion Fe2+ dikarenakan potensial reduksinya yang lebih rendah dibanding oksigen (O2). Proses oksidasi ini terus berlanjut hingga akhirnya besi membentuk senyawa hidrat besi oksida Fe2O3.xH2O. Senyawa inilah yang kita kenal sebagai karat, yang biasanya berwarna kecoklatan dan membuat penampakkan besi menjadi kusam. Karat ini, selain merusak keindahan besi, lambat laun juga bisa merusak besi tersebut.
Pencegahan Korosi
Karena berbagai macam kerugian yang disebabkan oleh karat, maka kita ditantang sebisa mungkin untuk mencegah terjadinya proses korosi pada besi. Ada banyak cara telah dikembangkan untuk mencegah proses korosi ini. Penggunaan metode pencegahan disesuaikan dengan peruntukan untuk apa besi digunakan.
Salah satu cara terbaik untuk mencegah korosi adalah dengan memadukan (alloying) besi dengan logam lain. Misalnya, besi dapat dipadukan dengan unsur krom dengan kadar paling sedikit 12%. Perpaduan ini menghasilkan logam yang kita kenal dengan nama stainless steel. Penambahan unsur krom pada besi dapat membentuk thin protective layer Cr2O3, yang dapat mencegah interaksi besi dengan oksigen dan molekul air.
Namun, cara pencegahan korosi dengan memadukan logam (alloying) terasa masih sangat sulit dilakukan dan memerlukan biaya yang tidak murah. Memadukan logam memerlukan tempat khusus dan pengawasan yang ketat. Belum lagi pengawasan kualitas paduan yang juga memerlukan ketelitian.
Oleh karenanya, perlu ada cara-cara yang lebih sederhana, mudah, dan murah yang bisa dilakukan untuk bisa mencegah korosi. Sebenarnya beberapa metode pencegahan sederhana sudah ditemukan dan digunakan secara luas.
Misalnya, dengan mengecat besi, memberikan oli dan gemuk, atau melapisi besi dengan logam lain (contohnya, pelapisan logam timah pada kaleng). Semua metode ini dilakukan dengan tujuan mencegah terjadinya interaksi besi dengan oksigen dan molekul air.
Pencegahan korosi dengan meniadakan interaksi besi dengan oksigen dan molekul air bisa kita kategorikan sebagai metode-metode fisis yang bisa kita lakukan. Selain metode fisis, pencegahan korosi juga bisa dilakukan dengan metode kimiawi.
Metode kimiawi dilakukan dengan cara mencegah terjadinya oksidasi pada besi meskipun besi berinteraksi dengan oksigen dan molekul air. Sebenarnya, membuat paduan logam bisa juga kita kategorikan ke dalam metode ini.
Ada beberapa metode kimiawi yang lebih mudah dilakukan. Salah satu metode yang sering dilakukan adalah galvanisasi. Galvanisasi adalah proses pelapisan besi dengan zink (seng). Pelapisan ini memiliki fungsi hampir mirip dengan pelapisan timah pada kaleng, dimana besi terlindungi dari interaksi dengan oksigen dan molekul air.
Namun, galvanisasi tidak hanya melindungi besi dengan cara fisis, ada proses kimianya juga, yang disebut dengan perlindungan katoda (cathodic protection). Perlindungan katoda terjadi karena zink memiliki potensial reduksi yang lebih negatif dibandingkan besi. Hal ini menyebabkan zink akan mengalami oksidasi di anoda menggantikan besi. Sehingga besi akan terlindungi dengan menjadi katoda yang mengalami reduksi.
Prinsip perlindungan katoda ini juga digunakan pada proses pelapisan kromium (chromium plating) untuk mendapatkan lapisan perlindungan karat yang mengilap sehingga lebih indah estetikanya.
Metode lain yang sering digunakan adalah pengorbanan anoda (sacrificial protection). Prinsipnya sama dengan prinsip perlindungan katoda dimana digunakan logam lain yang memiliki potensial reduksi lebih negatif dibandingkan besi.
Cara ini dilakukan dengan menghubungkan besi dengan logam yang lebih negatif potensial reduksinya itu dengan sebuah kawat. Ketika proses elektrokimia terjadi, logam besi akan tereduksi sehingga aman dari korosi. Di sisi kawat lain, logam yang menjadi anoda akan teroksidasi dan lama-kelamaan akan mengikis habis. Proses ini seolah membiarkan anoda teroksidasi dan terkikis. Hal inilah yang membuat metode ini diberi nama pengorbanan anoda.
Dengan berjalannya waktu, logam di anoda yang rusak bisa digantikan dengan yang baru sehingga proses perlindungan katoda masih tetap bisa berlangsung. Proses pergantian inilah yang membedakan metode ini dengan metode perlindungan katoda biasa. Metode ini banyak digunakan untuk melindungi korosi pada kapal laut dan pipa besi yang ditanam di dalam tanah.
Sebuah Refleksi
Meskipun peristiwa korosi besi adalah peristiwa yang terlihat merugikan, tetapi ada banyak hikmah yang bisa kita dapatkan dari adanya proses ini. Korosi besi menyebabkan diri kita ditantang untuk lebih banyak berpikir alternatif cara untuk mencegahnya.
Ketika kita mulai berpikir akan hal ini, ternyata kita justru diuntungkan dengan ditemukannya logam stainless steel yang lebih baik kualitasnya. Kita juga bisa menjadikan besi menjadi lebih memiliki nilai guna dan nilai estetika yang lebih tinggi dengan adanya pengecatan dan pelapisan dengan logam lain.
Hikmah ini kita dapatkan dari hanya memikirkan satu karakteristik dari logam yaitu karakteristik mudah mengarat. Sejatinya masih banyak karakteristik logam yang lain yang bisa kita pikirkan. Siapa tahu, ketika kita memikirkannya, kita akan mendapatkan hal-hal baru yang tidak pernah terbersit dalam pikiran kita sebelumnya.
Alhasil, proses korosi pada besi adalah hanya salah satu tanda kebesaran Tuhan yang Mahakuasa. Dari sini kita akan lebih memahami lagi, bahwa tidak ada yang diciptakan Tuhan tanpa adanya hikmah, walaupun terkadang di mata manusia ciptaannya tersebut terlihat merugikan.