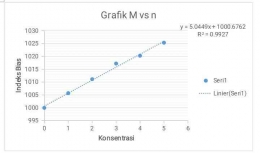
Semakin besar molalitas sebuah larutan, maka nilai penurunan titik beku nya akan semakin tinggi. Sedangkan jika molalitas sebuah larutan semakin kecil, maka nilai penurunan titik bekunya akan semakin rendah pula ( Puspita.,2013).
Penjelasan diatas adalah sebagai pengertian awal dalam praktikum yang saya lakukan, maka dalam penentuan berat molekul berdasarkan penurunan titik beku, maka berikut adalah alat, bahan, dan prosedur yang saya gunakan yaitu:
- Alat- Alat Yang Digunakan Sebagai Berikut:
1. Termometer 100 C (1 buah)
2. Tabung Reaksi Besar (2 buah)
3. Pengaduk (2 buah)
4. Gelas Kimia 800 ml (1 buah)
5. Gelas Kimia 250 ml (2 buah)
6. Spatula (1 buah)
7. Kaca Arloji (1 buah)
8. pipet Tetes (2 Buah)
- Bahan Yang Digunakan
- Benzena (Cair, Tidak Berwarna, 20 ml)
- Asam Benzoat (Padat, Putih, 0,15 gram)
- Es balok (Padat, Tidak Berwarna, Secukupnya)
- Prosedur Kerja
- Disiapkan gelas kimia dan tabung reaksi besar lalu ditimbang.
- Dimasukkan 20ml benzena kedalam tabung reaksi besar yang sudah ditimbang dan ditimbang kembali.
- Dimasukkan tabung reaksi tersebut kedalam gelas kimia yang sudah berisi es batu, lalu diaduk cairan secara perlahan dan merata.
- Dicacat harga suhu setiap selang waktu 0,5 menit (30 detik). Percobaan dihentikan setelah 10 kali selang waktu 0,5 menit, maka diperoleh harga suhu yang tetap dan dirata-ratakan semua suhu yang diamati.
- Ditimbang 0,5 gram asam benzoat, kemudian dimasukkan kedalam pelarut murni benzena.
- Ditentukan titik beku larutan asam benzoat dengan cara percobaan 4, lalu dihitung perbedaan titik beku pelarut dan titik beku larutan.
-
Beri Komentar
Belum ada komentar. Jadilah yang pertama untuk memberikan komentar!