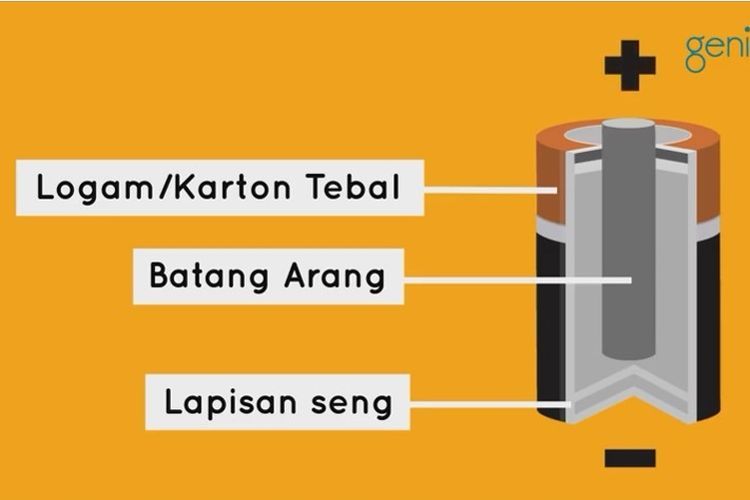
Ya, baterai adalah contoh aplikasi sel volta yang paling banyak digunakan. Baterai yang sering kita gunakan dinamakan bateri kering atau baterai Leclanche. Nama Leclanche merujuk pada ilmuwan yang menemukan baterai ini pada tahun 1866.
Baterai kering menggunakan seng (Zn) sebagai anoda, sedangkan pada katoda terdapat elektroda inert, yaitu grafit yang dicelupkan di tengah-tengah pasta. Pasta ini mengandung batu kawi (MnO2) yang berfungsi sebagai oksidator.
Prinsip kerjanya, Zn akan teroksidasi mengeluarkan elektron yang kemudian ditangkap MnO2 sehingga tereduksi menjadi Mn2O3. Reaksi redoks ini menyebabkan adanya potensial kira-kira sebesar 1,5 volt.
Prinsip sel volta, juga digunakan pada aki. Aki adalah sumber energi penting untuk kendaraan kita. Aki bisa menghasilkan beda potensial yang lebih besar dari baterai. Bahkan rangkaian pada sel volta aki bisa dihubungkan secara seri untuk menghasilkan potensial yang lebih besar.
Pada aki, yang bertindak sebagai anoda adalah timbal (Pb), dan yang bertindak sebagai katoda adalah timbal (IV) oksida (PbO2). Kedua elektroda dicelupkan ke dalam larutan asam sulfat (H2SO4) sebagai medium tempat terjadinya reaksi redoks.
Dalam satu sel aki kira-kira dihasilkan potensial sebesar 2 volt. Namun, jika dihubungkan secara seri, potensial bisa dinaikkan tergantung berapa sel yang digunakan.
Setelah digunakan, baterai dan aki ini akan berhenti bekerja karena terjadi pengosongan sehingga tidak terjadi reaksi redoks lagi. Namun pada beberapa sel volta bisa dilakukan pengisian kembali (recharge).
Hal ini yang menyebabkan sel volta bisa diklasifikasikan menjadi dua, yaitu sel primer dan sel sekunder. Sel primer adalah sel volta sekali pakai atau tidak bisa diisi ulang, sedangkan sel sekunder sel volta yang bisa diisi ulang. Baterai kering adalah salah satu contoh sel primer, sedangkan aki adalah salah satu contoh sel sekunder.
Proses pengisian aki sangat sederhana. Caranya dengan membalikkan reaksi yang terjadi pada elektroda dengan menggunakan sumber arus. Anoda dihubungkan dengan kutub negatif, dan katoda dengan kutub positif sehingga elektroda akan kembali ke kondisi semula dan siap untuk dipakai kembali.
Sebuah Refleksi
Proses ditemukannya baterai dan aki dimulai dari pengamatan pada reaksi yang terjadi di alam. Terjadinya berbagai reaksi di alam bukan tanpa hikmah. Semua itu menunjukkan kebesaran Tuhan yang Mahakuasa di dunia ini baik secara eksternal maupun internal.
Secara eksternal maksudnya adalah kita bisa melihat bagaimana segala sesuatunya tertata rapi di dunia, dan semuanya bisa digunakan untuk kemaslahatan umat manusia. Kuncinya berada pada diri kita sebagai manusia, apakah kita mau menelitinya atau tidak, apakah kita mau menggali kedalaman hakikatnya atau tidak.
Beri Komentar
Belum ada komentar. Jadilah yang pertama untuk memberikan komentar!