Pada tahu ga NaCl itu apa? Pada ngeh ga Natrium klorida itu apa? Duh geleng-geleng ya! Ganti deh pertanyaannya, pada tahu ga garam dapur? Pasti pada nganguk-ngangguk tahu.
NaCl (Natrium Klorida) atau garam dapur itu senyawa yang sama Bwambaaaaang! Ketemu tiap hari tapi ga ngerti rumus kimianya macam mana.
Hm...tapi ga usah panik atau berisik, banyak kok yang merasa entah berantah kalau disodori rumus atau senyawa kimia.
Mari saya beri pencerahan sedikit tentang tata nama senyawa kimia ini.
Tata nama senyawa kimia terbagi dua, senyawa yang terbentuk dari unsur non logam dan non logam, satu lagi senyawa yang terbentuk dari unsur logam dan non logam.
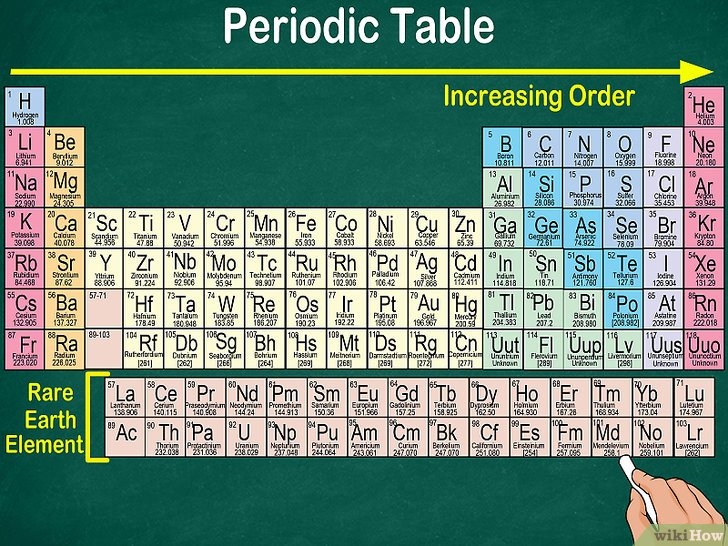
Nah loh unsur logam dan logamnya pegimane nih bingung. Unsur logam itu golongang IA yang terdiri dari Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cesium (Cs), Fransium (Fr), lalu golongam IIA ada Berilium (Be), Magensium (Mg), Kalsium (Ca), Stronsium (Sr), Barium (Ba), dan Radium (Ra) lalu di IIIA hanya Alumunium yang dikategorikan logam.
Ada juga golongan logam transisi, seperti Scandium (Sc), Titanium (Ti), Vanadium (V), Crom (Cr), Mangan (Mn), Besi/ Fero (Fe), Kobalt (Co), Nikel (Ni), Cuprum/ Tembaga (Cu) dan Seng/Zinc (Zn).
Nah selain itu golongan IIIA,IVA,VA,VIA,VIIA,VIIA termasuk non logam. Karena banyak, kita ngafalinnya selain IA,IIA, Al dan transisi yang lainnya non logam.
Tata Nama Senyawa Non Logam dan Non Logam
Kita bahas yang gampang dulu ya. Kenapa gampang? Karena cara menyebutkan atau menuliskan nama senyawa yang terdiri dari non logam dua-duanya simpel, yaitu:
Sebutkan jumlah dan nama unsur non logam yang paling depan (kecuali jumlahnya satu ga usah disebut), lalu jumlah dan nama unsur non logam kedua dengan menambahkan akhiran "ida" di belakang nama unsur kedua tersebut. Misal oksigen jadi oksida, klor jadi klorida.
Nah jumlahnya sendiri sebutannya 1 adalah mono, 2 itu di, tiga kita sebut tri, empat disebut tetra, lima itu penta dan 6 itu heksa.
Contoh pemberi nama tata nama senyawa non logam dan non logam, misalnya:
Beri nama CO dan CO2
C dan O terdiri dari Karbon (non logam) dan Oksigen non logam
Maka, untuk CO kita beri nama Karbon monoksida karena oksigennya hanya 1. Sementara pada CO2 karena ada 2 oksigennya, maka namanya menjadi karbon dioksida.
Contoh lain, yaitu NO, NO2, N2O4, san N2O5
N adalah nitrogen golongan VA berarti non logam, dan O alias oksigen golongan VIA juga non logam, maka tata namanya adalah sebagai berikut:
NO: Nitrogen Monoksida
NO2: Nitrogen Dioksida
N2O4: Ada dua nitrogen, yaitu Dinitrogen dan ada 4 oksigen sebagai unsur non logam, kedua jadi tetra oksida maka namanya Dinirogen Tetraoksida.
N2O5: Ada dua nitrogen sebagai unsur pertama Dinitrogen dan ada 5 oksigen sebagai unsur non logam, kedua jadi pentaoksida maka namanya Dinitrogen Pentaoksida
Nah tata nama untuk senyawa kedua ini tidak lah semudah tata nama senyawa non logam dan non logam. Jadi kalau nanti belajar ini langsung puyeng ya dimaafkan.
Tata nama senyawa logam dan non logam terbagi lagi menjadi dua. Senyawa dengan logam yang biloknya hanya 1 saja dan senyawa dengan logam yang memiliiki biloks banyak.
Sekilas info, biloks adalah bilangan oksidasi yang menunjukan kemampuan melepas atau menerima elektron suatu atom jika muatannya + / plus maka dia cenderung lepas, sementara - / minus dia cenderungnya terima elektron.
Untuk membantu perhitungan bilok biasanya kita menggunakan bilok Oksigen (O) sebesar -2, atau Hidrogen (H) +1.
Tata Nama Senyawa Logam dan Non Logam untuk Logam dengan Bilok Satu
Penamaannya terbagi lagi menjadi diatomoik atau poliatomik
Diatomik
Diatokik adalah senyawa yang terdiri dari dua atom saja
Unsur logam yang meniliki biloks satu adakah golongan IA dengan biloks 1 dan golongan IIA dengan biloks +2 serta Alumunium Al dengan biloks + 3. Selain itu maka biloknya lebih dari seperti golongan transisi.
Nah, cara menyebutkan atau menuliskan namanya adalah sebagai berikut:
Nama unsur logam lalu nama unsur non logam yang diberi akhiran "ida"
Contoh: beri nama NaCl, CaCl2, AlCl3
Nah baik NaCl, CaCl2 maupun AlCl3 merupakan senyawa dengan unsur logamnya memiliki biloks hanya satu.
NaCl, Na (Natrium biloks +1) dan Cl (klor)
Maka kita sebut Natrium Klorida
CaCl2
Ca (kalsium golongan IIA biloks +1) dan Cl (klor)
Maka kita sebut Kalsium Klorida
AlCl3
Al (Aluminium golongam IIIA biloks +3) dan Cl (klor)
Maka kita sebut Alumunium Klorida
Perhatikan perbedaannya dengan tata nama senyawa non logam dan non logam di mana jumlah disebutkan, pada tata nama senyawa logam dan logam tidak perlu disebutkan jumlah Cl atau klornya.
Poliatomik
Poliatomik artinya senyawa yang terdiri lebih dari 2 atom. Namun tidak usah khawatir karena unsur sesudah logam itu adalah ion di mana namanya sudah ada tinggal menghapal saja.
Contoh SO4 2- itu adalah sulfat, NO3- adalah nitrat, lalu PO4 3- adalah psofat dan banyak lagi contoh ion yang sudah paten namanya.

Na2SO4 , K3PO4 dan Ca(NO3)2
NaSO4 namanya adalah Natrium Sulfat
K3PO4 adalah Kalium Posfat
Dan Ca(NO3)2 adalah Kalsium Nitrat
Tata Nama Senyawa Logam dan Non Logam untuk Logam dengan Bilok Lebih dari Satu
Diatomik:
Tata nama senyawanya adalah unsur logam kemudian tunjukan biloknya dalam kurung setelah penyebutan logam, namun angkanya ditulis dalam huruf romawi, kemudian unsur non logam berikan akhiran "ida".
Contoh: Fe2O3
Oksigen memiliki biloks -2 karena ada 3 jumlahnya, maka oksigen memiliki total bilok -6. Agar muatan nol, maka besi total bernuatan +6 karena besi ada 3 maka jika kita bagi 2 bilok untuk satu besi adalah + 3 maka namanya besi (III) oksida.

Unsur logam kenudian tunjukan biloknya dalam kurung setelah penyebutan logam namun angkanya ditulis dalam huruf romawi, kemudian nama senyawanya.
Contoh:
ZnSO4: Zn itu adalah seng sementara SO4 adalah sulfat.
Karena SO4 muatannya -2 , maka agar kedua senyawa bermuatan netral seng bermuatan + 2 maka namanya seng (II) sulfat.