Setelah calon obat terbukti berkhasiat dan aman, barulah obat tersebut dizinkan untuk diproduksi oleh industri dan dipasarkan. Tentunya sebelum dipasarkan, obat baru tersebut harus didaftarkan dan dievaluasi lebih dulu oleh pihak otoritas terkait. Misalnya BPOM (Indonesia), US FDA (Amerika Serikat), TGA (Australia), MHRA (Inggris), dan lainnya.
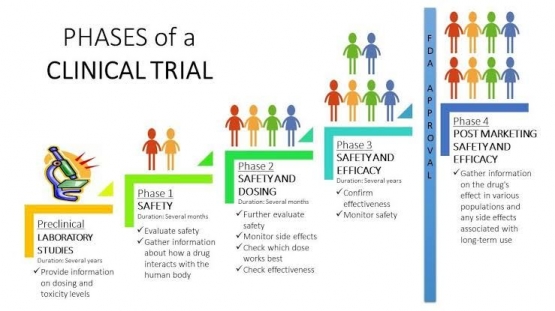
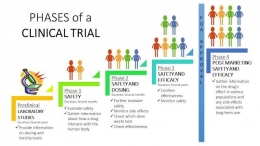
Uji Klinik Fase IV dilakukan setelah obat dipasarkan, sehingga disebut juga dengan Studi Pasca-Pemasaran (Post-Market Surveillance). Mengapa? Bukankah obat yang sudah dipasarkan berarti sudah disetujui oleh otoritas terkait dan terjamin khasiat dan keamanannya?
Jadi begini, walaupun suatu obat baru telah lulus serangkaian penelitian dan pengujian yang ketat, tapi ketika obat tersebut dikonsumsi oleh seluruh orang dunia dengan usia dan ras yang beragam, itu berarti cakupan pemakainya lebih luas lagi. Maka bisa jadi ada efek samping tertentu yang tidak muncul saat Uji Klinik sebelumnya.
Oleh sebab itu, pasien yang mengalami efek samping yang tidak disebutkan dalam brosur obat, wajib melaporkan kepada produsen atau pihak otoritas terkait. Hal ini disebut juga dengan istilah Farmakovigilans.
Jika ada banyak laporan dan dinilai obat tersebut membahayakan, bukan tidak mungkin obat tersebut akan ditarik dari peredaran (recall). Beberapa contoh obat yang ditarik dari peredaran setelah obat tersebut beredar di pasar misalnya, Cerivastatin (Antihiperkolesterolemia) ditarik karena dapat merusak ginjal (nefrotoksik), Talidomid (antimual) yang dapat menyebabkan cacat janin (teratogenik), dan lainnya.
Mematenkan Obat Baru
Setelah viralnya tanaman Bajakah ini, diberitakan banyak muncul seruan untuk mematenkan tanaman tersebut. Perlu dicatat bahwa mematenkan suatu obat tujuannya lebih terkait ke komersil. Tentunya selama proses penelitian yang begitu lama, suatu perusahaan telah mengeluarkan banyak sekali biaya.
Jangan membayangkan proses ini berjalan sangat mulus tahap demi tahap. Proses ini bisa memakan waktu belasan hingga puluhan tahun. Dimulai dari penentuan senyawa (secara sintetis atau mengambil isolat dari bahan alam), formulasi, uji stabilitas, dan seterusnya hingga Uji Klinik selesai.
Setiap tahapan bisa jadi harus diulang berkali-kali. Itulah mengapa pengembangan obat baru biasanya lebih lambat daripada perkembangan penyakit baru, karena waktu yang dibutuhkan untuk penemuan obat baru memang sangat lama dan membutuhkan modal yang tinggi. Hal ini tentunya menjadi tantangan tersendiri di dunia kesehatan.
Jadi boleh dikatakan Paten menjadi suatu hak eksklusif suatu pihak yang telah berhasil menemukan senyawa atau obat baru tersebut. Tidak heran juga, harga obat originator (istilah untuk menyebut obat baru yang sudah dipatenkan) biasanya sangat mahal. Masa paten umumnya berlangsung 20 tahun. Jadi selama masa paten belum berakhir, siapapun tidak boleh memproduksi obat yang sama.
Jika tanaman Bajakah hendak dipatenkan sebagai obat baru untuk menyembuhkan kanker, tentunya merupakan suatu hal yang luar biasa. Namun seperti yang sudah banyak diberitakan, Bajakah mengandung banyak sekali senyawa Fitokimia. Nah, pihak inventor harus menentukan secara spesifik senyawa apa saja yang benar-benar memiliki khasiat sebagai antikanker, berapa dosisnya, bentuk sediaannya, dan lain sebagainya.
Semoga pembaca sekalian kini bisa memahami kira-kira sepanjang apa perjalanan yang harus dilalui oleh suatu obat baru untuk dapat diklaim dapat menyembuhkan penyakit. Seluruh tahap ini tentunya untuk memastikan Safety (keamanan), Efficacy (khasiat) dan Quality (mutu) obat.