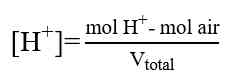
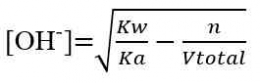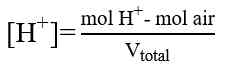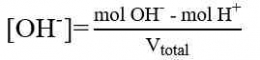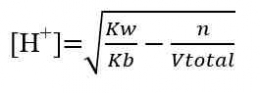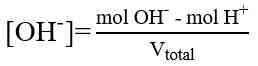M = Molaritas asam atau basa
V = Volume asam atau basa
Contoh:
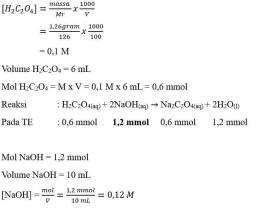
Larutan standar dibuat dari 1,26gram kristal asam oksalat dihidrat (H2C2O4.2H2O) yang dilarutkan dengan aquades dalam labu ukur 100 mL dan diencerkan sampai tanda batas. Larutan ini sebagai titran untuk menitrasi 10 mL larutan NaOH. Volume asam oksalat yang diperlukan sampai titik ekuivalen adalah 6 mL. Tentukan konsentrasi larutan NaOH.
Jawab:
Pada saat tercapai titik ekuivalen, perbandingan mol zat-zat yang bereaksi sama dengan perbandingan koefisiennya, maka: Dokpri
Dokpri
na . Ma . Va = nb . Mb . Vb
2 x 0,1 M x 6 mL = 1 x M x 10 mL
[NaOH] = 1,2 mmol/10 mL = 0,12 M
Grafik Titrasi Asam Basa
1. Titrasi Asam Kuat-Basa Kuat
Beri Komentar
Belum ada komentar. Jadilah yang pertama untuk memberikan komentar!