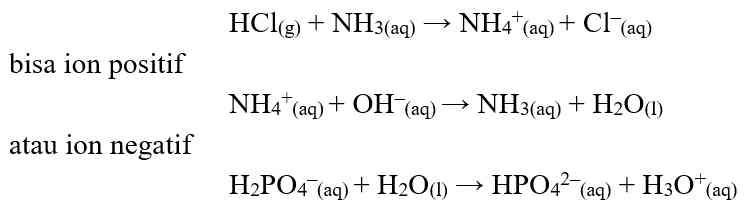Dokpri
Dokpri
Pada reaksi antara H+ dan NH3, H+ bertindak sebagai asam, sedangkan NH3 bertindak sebagai basa.
Teori asam basa Lewis lebih luas daripada teori asam basa Arrhenius dan teori asam basa Bronsted-Lowry. Hal ini disebabkan
1. Teori Lewis dapat menjelaskan reaksi asam basa dalam pelarut air, pelarut selain air, bahkan tanpa pelarut.
2. Teori Lewis dapat menjelaskan reaksi asam basa tanpa melibatkan transfer proton (H+), seperti reaksi antara NH3 dengan H+
Baca konten-konten menarik Kompasiana langsung dari smartphone kamu. Follow channel WhatsApp Kompasiana sekarang di sini: https://whatsapp.com/channel/0029VaYjYaL4Spk7WflFYJ2H
Beri Komentar
Belum ada komentar. Jadilah yang pertama untuk memberikan komentar!