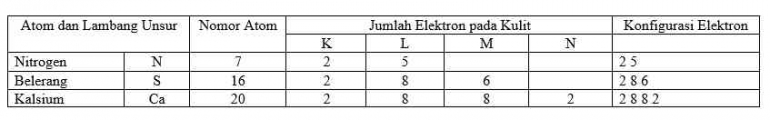
Kulit K = 2 (jumlah maksimum kulit pertama)
Kulit L = 8 (jumlah maksimum kulit kedua)
Kulit M = 8 (kulit terluar tidak boleh melebihi 8 elektron)
Kulit N = 2 (tersisa 2 elektron)
Sehingga konfigurasi elektronnya 2) 8) 8) 2)
Melalui konfigurasi elektron, golongan dan periode suatu atom dapat diketahui, dimana golongan ditentukan oleh jumlah elektron terluar (elektron valensi) dan periode ditentukan dari nomor kulit terbesar yang berisi elektron valensi.
2. Konfigurasi Elektron Berdasarkan Subkulit
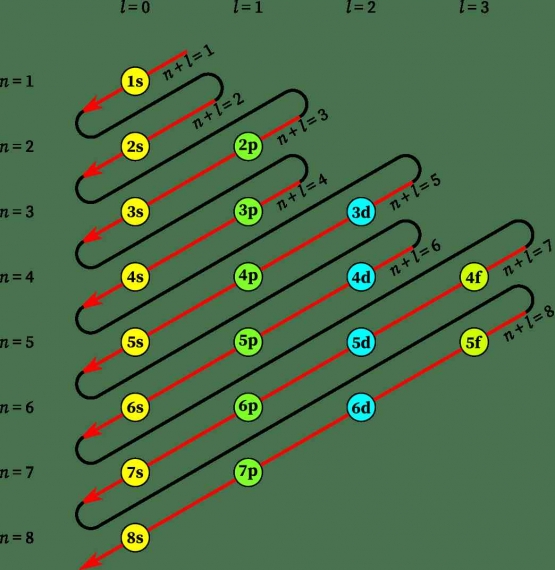
Pada konfigurasi elektron berdasarkan kulit, terjadi penyimpangan aturan terhadap logam transisi yang dapat diatasi dengan konfigurasi elektron berdasarkan subkulit. Penulisan konfigurasi berdasarkan subkulit menurut model mekanika kuantum menggunakan diagram orbital yang mempertimbangkan tiga aturan (asas), yaitu Asas Aufbau, Asas Larangan Pauli, dan Asas Kaidah Hund.
1) Asas Aufbau
Aufbau berasal dari kata Jerman "Aufbau" yang berarti membangun. Prinsip Aufbau mengatakan bahwa: "Apabila proton ditambahkan satu per satu ke dalam inti atom untuk membentuk suatu unsur, maka dengan cara yang sama elektron juga ditambahkan ke dalam orbital-orbital atomnya". Dengan demikian, konfigurasi elektron dilakukan dalam keadaan standar, dimana pengisian elektronnya dimulai dari subkulit yang memiliki tingkat energi rendah ke tingkat energi yang lebih tinggi, sehingga atom berada pada tingkat energi yang minimum.